
COMING SOON

DATI CLINICI
Synergo® - Articoli sul trattamento adiuvante (profilattico):
Studio clinico controllato randomizzato: 83% liberi da malattia al follow-up a 2 anni (Colombo et al.)
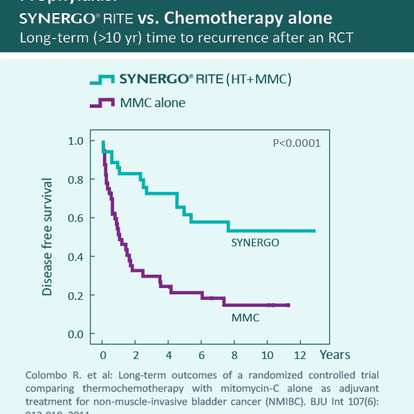
Follow-up a lungo termine: 53% liberi da malattia al follow-up a 10 anni (Colombo et al. 2003), 72% liberi da malattia al follow-up a 10 anni (Moskowitz et al. 2012)
Pazienti con fallimento di BCG: 72% liberi da malattia al follow-up a 2 anni (Native et al. 2009)
Studio clinico controllato randomizzato: 78,3% liberi da malattia al follow-up a 2 anni (Arends et al.)
Candidati per la cistectomia: 85% e 48% liberi da malattia al follow-up a 1 anno e 2 anni rispettivamente (Volpe et al.)
Pazienti T1G3: 57,1% liberi da malattia al follow-up a 2 anni (Halachmi et al.)
Synergo® - Articoli sul trattamento neo-adiuvante (ablativo):
Tassi di risposta completa (eliminazione del tumore) rilevati con trattamento Synergo® (3-24mesi follow-up):
72% (Nair 2014)
85% (Luedecke 2014)
79% (Moskowitz 2012)
92% Risposta completa (Witjes 2009) Carcinoma in situ: 51% liberi da malattia al follow-up a 2 anni (Witjes et al.)
75% (Gofrit 2003).



>35.000
TRATTAMENTI TERAPEUTICI EFFETTUATI
>50
STUDI CLINICI E SCIENTIFICI PUBBLICATI
12
PAESI
Dall’inizio nel 1991 e interrottamente fino a oggi, sono stati condotti studi clinici per esaminare i benefici del trattamento combinato di Synergo® rispetto alle sole chemioterapia e immunoterapia, per pazienti con NMIBC e altri tumori a carico della vescica. I risultati positivi hanno condotto allo sviluppo di “Synergo®” e “trattamento Synergo®”.
Molti centri hanno pubblicato ulteriore documentazione e avviato il trattamento di routine dei loro pazienti con Synergo®.
Migliaia di pazienti sono stati sottoposti al trattamento nel corso degli anni e sono stati attentamente monitorati per eventuali effetti collaterali e complicazioni. La maggior parte degli effetti collaterali e delle complicazioni osservate sono ben conosciuti e già associati alle instillazioni di chemioterapia intravescicale (senza ipertermia). Gli effetti collaterali osservati erano transitori e generalmente senza ripercussioni a lungo termine sulle funzioni della vescica, erano di carattere superficiale e si sono risolti nel corso del trattamento con un intervento medico minimo e senza effetti residui rilevanti. Le complicazioni osservate sono state trattate in maniera soddisfacente utilizzando procedure standard. Effetti collaterali simili si sono verificati durante i trattamenti Synergo® Coadiuvante (profilattico) e Neoadiuvante (ablativo). Il trattamento Synergo® con ipertermia e chemioterapia non causa complicazione grave, ad eccezione degli eventi anticipati che si verificano a seguito di cateterizzazione della vescica urinaria e di trattamento con ipertermia e chemioterapia. Di conseguenza, il trattamento eseguito con il sistema Synergo® può essere considerato sicuro e non comporta alcun rischio per il paziente o per l’operatore. Gli effetti collaterali sono documentati e presentati in riviste scientifiche pubblicate.
GLI ESPERTI CONDIVIDONO

Prof. Dr. med. J.A. Witjes PhD MD
Radboud UMC, Nijmegen, The Netherlands
“I have seen remarkable responses in these patients in spite of their being in the list for a cystectomy”

Dr. med. Gerson Lüdecke Head of Uro-Oncology section
University Clinics of Giessen-Marburg, Germany
"Synergo is a pioneering therapy ready for fast track implementation in urology. With more than 10 years of Synergo experiences in high risk NMIBC we achieved minimal recurrence rates using it alternatively to BCG with negligible side effects, and in BCG-failing patients who were externally discussed for cystectomy, we were impressed with the high bladder preservation rate"

Prof. Dr. med. Sanjeev Madaan PhD MS Dip NB FRCS (urol) FEBU
Dartford and Gravesham NHS Trust, Kent , UK
"I have been using Synergo RITE for many years and have found it extremely useful in the management of high-risk NMIBC patients who have failed intravesical BCG and are not keen or suitable for cystectomy"
Mr Ahmed Ali
MBChB, MSc Urology, FRCS Urol
Frimley Health NHS Foundation Trust UK
"The Synergo system has helped us deliver individualised cancer care for patients with high risk NMIBC. The long-term data supports the use of the technology in many indications and help patients making an informed choice in respect to bladder preservation treatment"

Prof. Dr. med. Renzo Colombo FEBU, BC Head of Lombardy Oncology Network
San Raffaele Hospital, Milan, Italy
"I have been working with the Synergo technology since it's development, and for over 20 years have seen very pleasing results in terms of oncological outcome and in the patients 'quality of life"

Prof. Dr. med. Shahrokh F. Shariat PhD MD
Professor and Chairman of Department of Urology, Medical University Vienna, Austria
“Having witnessed its clinical benefits for several years, I think that Synergo will play a significant role in the management of NMIBC.”

Prof. Dr. med. Ofer Nativ PhD MD,
Chairman of Urology Department Bnai-Zion Medical Center, Haifa, Israel
“I have been using Synergo technology for over a decade now and I am satisfied with the results, especially in high risk patients (CIS, T1, high grade and BCG failures). I was able to appreciate its ablative potency and remarkably low dropout rate.”

Prof. Dr. med. Dr. phil. Thomas Bschleipfer FEBU, PhD MD,
Head Urology Department
Klinikum Weiden, Weiden, Germany
“The Synergo® RITE is a highly effective instrument to lower the otherwise extraordinary hazard of high risk NMIBC. It assures an excellent treatment response and thus, gives many of our patients a much better quality of life.”

Mr Rami Issa MD FRCS (Urol) CABU FEBU
St George's University Hospitals, London, UK
"For more than 10 years in our hospital, Synergo proved to be a very helpful option for the difficult group of approx. 200 patients, so far, with High Risk NMIBC, who did not respond to other intravesical therapies. We've saved many bladders over these 10 years!"
LA SCIENZA DEL ENERGIA RF
La distruzione dei tessuti tramite calore è un fenomeno noto da tempo [1]. La spiegazione più comunemente accettata per l’utilità dell’ipertermia nel trattamento del cancro di per sé e in combinazione con altre forme di trattamento è legata alla differenza nella vascolarizzazione dei tumori rispetto al tessuto normale [2].
I tumori crescono nei tessuti raggiunti da vascolarizzazione preesistente. Quando il tumore cresce, lo fa a scapito della normale circolazione del sangue.
Effetti sinergici di regressione dei tumori sono stati osservati nei casi in cui l’ipertermia viene utilizzata assieme ad agenti antineoplastici selezionati. Il meccanismo della regressione sinergica del tumore può essere spiegato da un aumento dell’uptake cellulare del farmaco, dall’alterazione della distribuzione intracellulare e del metabolismo del farmaco e da un aumento della velocità di reazione del farmaco. L'obiettivo del sistema Synergo è raggiungere all'interno dei tessuti una temperatura adatta per consentire al farmaco di penetrare meglio, accelerandone la reazione con il DNA.
Si sono rilevati livelli plasmatici di mitomicina C incrementati di 6 volte quando il farmaco viene instillato intravescicalmente utilizzando il sistema Synergo® [3].
La penetrazione di MMC nella parete della vescica e delle cellule può essere spiegata con le correnti elettriche Inter e intracellulari di droga-mobilitazione ("Foucault") prodotte dalla radiazione RF e la fornitura di calore profonda molto efficiente. Le stesse correnti sono anche responsabili della "micro-Poring"[4] della membrana cellulare che aumentano l'assorbimento del farmaco, a causa del trasferimento ionico.
Uno studio recente[5] presenta che RF causa i declini nella vitalità e nella proliferazione delle cellule tumorali, cambia la funzione dei mitocondri nelle cellule tumorali ed è stato seguito dall'altezza di autophagosomes nel citoplasma delle cellule tumorali. D'importanza, gli effetti del trattamento di RF erano trascurabili in cellule non-maligne.
Un modello distinto di risposta immunitaria umorale e mediata da cellule, osservato unicamente nei pazienti trattati mediante MMC con Synergo® RITE [6-7] può anche essere un fattore che contribuisce ai livelli abbastanza bassi di recidiva e di valori di progressione riportati, anche nei pazienti ad alto rischio [8-12].
[1] Storm, F.K., et al. Cancer Res 39, 2245-51 (1979).
[2] Natadze, T.G. Vopr Onkol 5, 654-62 (1959).
[3] Paroni, R. et al. Br J Clin Pharmacol 52, 273-8 (2001).
[4] Ware et al. Scientific Reports | 5:12083 | 2015 43.
[5] Curely et al. Curley S. et al. Int. J. Environ. Res. Public Health 2014, 11, 9142-9153 (2014).
[6] Colombo, R. et al. J Urol 155, 1227-32 (1996).
[7] Colombo, R. et al. J Urol 153, 959-63 (1995).
[8] Witjes, J.A., et al. World J Urol 27, 319-24 (2009).
[9] Nativ, O. et al. J Urol 182, 1313-7 (2009).
[10] Halachmi, S. et al. Urol Oncol 29, 259-64 (2011).
[11] Gofrit, O.N. et al. Urology 63, 466-71 (2004).
[12] Kilb, J.-I. et al. Journal of Clinical Oncology 36, 456-456, doi:10.1200/JCO.2018.36.6_suppl.456 (2018).

Synergo local RF and chemotherapy (Thermo chemotherapy) for the treatment of patients with Bacillus Calmette-Guerin (BCG)-unresponsive
MODALITÀ DI TRATTAMENTO
Il Sistema Synergo® consente di utilizzare due modalità di trattamento
Trattamento Adiuvante (Profilattico) – serve a prevenire le recidive del tumore dopo il completamento della procedura chiamata Resezione Transuretrale del Tumore della Vescica (Transurethral Resection of Bladder Tumor – TURBT) nei pazienti a rischio elevato o intermedio, secondo le direttive dell’Associazione Europea di Urologia*.
Stadio patologico Ta-T1, papillare o solido.
Il trattamento consiste in 6 sessioni settimanali seguite da sessioni di mantenimento.
Trattamento Neo-Adiuvante (Ablativo) – serve ad estirpare il tumore. Per quei pazienti in cui l'estirpazione completa del tumore non può essere effettuata con un unico TURBT (sedi multiple e/o disturbi elevati per tumore); Carcinoma in Situ (CIS), per quei pazienti che non possono essere sottoposti ad anestesia per ragioni mediche; per quei pazienti che rimangono affetti da tumore nonostante il TURBT radicale o per quei tumori che sono irresecabili a causa dell'ubicazione anatomica inaccessibile.
Il trattamento inizia con 4 sessioni settimanali, a seguito delle quali i criteri di risposta vengono verificati tramite video-cistoscopia o biopsie. Se si ottiene una risposta parziale, il paziente viene sottoposto ad altre 4 sessioni settimanali. Dopo il completamento della risposta, il paziente inizia la modalità di trattamento adiuvante.
